Меню сайта
- На главную
- Рост растений
- Почвенные простейшие
- Полиморфизмы
- Дыхание бактерий
- Органическая природа
- Первая жизньу
- Материалы по биологии
Последние новости
Причина отравления вод океана.
Американские ученые из штата Мичиган полагают, что в качестве главной причины отравления вод Мирового океана ртутью являются бактерии.
Секрет выживания лягушек.
Американским ученым удалось выяснить, как лягушкам удается продолжать жить даже после глубокой заморозки.
Секрет долголетия ночницы.
Биологи уже давно считают, что продолжительность жизни животного определяется очень просто: чем оно больше, тем дольше живет.
Методы количественного анализа микробной популяции в природеМатериалы по биологии и химии / Кинетика микробного роста в природных экосистемах / Методы количественного анализа микробной популяции в природеСтраница 3
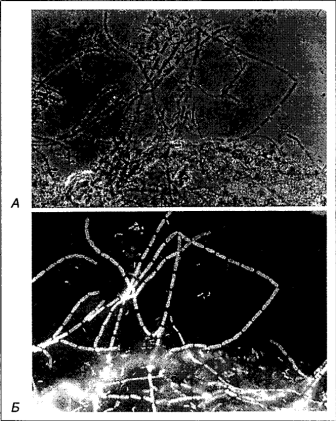
Рис. 3 - Определение протеобактерий с группоспецифическим нуклеотидным зондом к рРНК. А. Фазово-контрастная микроскопия. Б. Тот же препарат при флуоресцентной микроскопии с УФ-эпиосвещением
Этот метод дает чрезвычайно эффектные результаты при его сочетании с конфокальной лазерной микроскопией, позволяя одновременно визуализировать группы бактерий различного систематического уровня в виде трехмерной картины и выявлять, например, их пространственные взаимосвязи.
Применение полимеразной цепной реакции позволяет копировать даже единственную молекулу 16S-рРНК (в виде ДНК) в экстрактах из природных образцов для сравнения нуклеотидных последовательностей этой ДНК с ДНК известных прокариот. Таким способом предлагается изучать филогенетические связи некультивируемых бактерий с другими прокариотами. Амплифицированную ДНК можно использовать для создания зондов, специфичных к нуклеиновым кислотам неизвестных микроорганизмов, и таким образом оценивать разнообразие микробного сообщества, независимо от способности данных микроорганизмов расти в культуре. Этот же метод может быть использован для того, чтобы проследить судьбу некультивируемого организма при тех или иных способах изучения общей популяции, например в процессе получения накопительной культуры нового организма с неизвестными потребностями или при изменениях в популяциях некультивируемых бактерий, например активного ила, в результате стрессовых природных ситуаций.
Наряду с перспективностью методов молекулярных зондов для микробной экологии следует отметить и их ограничения. Эти методы позволяют установить присутствие определенного типа микроорганизмов и его принадлежность к той или иной ветви филогенетической системы, созданной на основе анализа последовательностей. Однако в большинстве случаев они не дают возможности определить экологическую нишу (тип метаболизма) некультивируемого организма, поскольку филогенетические группы не гомологичны метаболическим группам, даже на уровне мельчайших разветвлений системы. Кроме того, не все прокариоты одинаково доступны для применения молекулярных зондов. Некоторые бактерии, особенно обладающие толстыми клеточными стенками или окруженные капсулой либо слизью, остаются трудными объектами для экстракции ДНК или гибридизации РНК с зондами. Поскольку метод зондов к тому же селективен, определенные бактерии, возможно важные, при анализе популяций этим способом могут остаться незамеченными.
Заключение
Основным лимитирующим фактором в условиях природных экосистем для микроорганизмов является количество субстрата.
Механизмы устойчивости к голоданию включают увеличение числа высокоаффинных транспортных систем, увеличение клеточной поверхности, образование спор, уменьшение размеров клеток, адаптацию клеточного метаболизма путем синтеза индуцируемых голоданием белков и образование слизи.
Апробированные и разработанные простые модели искусственных экосистем (хемостаты) являются эффективным инструментом для изучения законов функционирования микробных популяций и их сообществ в природных экосистемах. При разработке подходов устойчивого развития биосферы экспериментальные и теоретические исследования позволяют выявить закономерности взаимодействия микробных популяций с остальными обитателями экосистем и найти подходы к управлению ими в моделях искусственных экосистем.
Однако все питательные среды и условия инкубации селективны для небольшой фракции общей бактериальной популяции, имеющейся в исследуемом образце; попытки составить менее специфические, более соответствующие природным условиям культуральные среды, позволяющие более точно оценивать разнообразие и численность микроорганизмов, пока не дали успеха.
Определение численности микроорганизмов в природных образцах можно осуществлять путем прямого подсчета под микроскопом флуоресцентно окрашенных клеток, радиоавтографии клеток, меченных 14С или 3Н, подсчета колоний, выросших на плотной питательной среде, определения роста в жидкой среде с учетом разведения, измерения общего содержания АТР, ДНК или более специфических клеточных компонентов, таких как жирные кислоты или хлорофилл, либо методами с применением флуоресцентно меченных антител. Все эти методы имеют свои ограничения.
Одиночные клетки или популяции микроорганизмов можно идентифицировать путем гибридизации с синтетическими рРНК-зондами или с рРНК-зондами, полученными на основе амплифицированной (методом ПЦР) ДНК. Эти методы можно применять в сочетании с оптическими для выявления в том числе некультивируемых микроорганизмов в природных образцах.
Смотрите также
Пространство в классической механике. Закон распространения теплоты Фурье
...
Лекарственные и ядовитые растения семейства Бобовые
Введение.
Общие сведения о бобовых
Бобовые
(лат. Fabaceae & Leguminosae, по плодам), или Мотыльковые (Papillionaceae,
по цветам) - название весьма обширного семейства растений из ...
Растительный мир Кольского полуострова
Введение
растительный мир полуостров
Учебная практика первого курса проходила на учебной базе МГТУ
расположенной в районе п.Тулома, на берегу реки Тулома, а так же на берегу
Верхнетуло ...